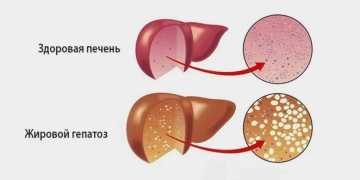
Гепатоз — это патологическое состояние, при котором возникает дистрофия гепатоцитов (основных клеток печени) в результате нарушения обменных процессов. Наиболее частой формой гепатоза является жировая дистрофия клеток или стеатоз. В норме в печени может содержаться небольшое количество жира. Проблема наступает тогда, когда его становится слишком много, то есть от 5 до 10% веса печени составляет жир. Это состояние называется стеатозом, его более тяжелая форма (с признаками воспаления печеночной ткани) называется стеатогепатитом.
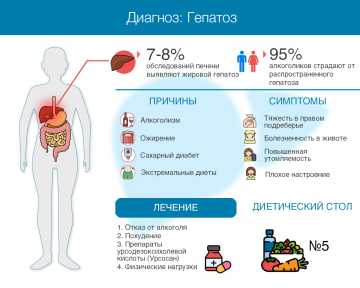
Если эти изменения не связаны со злоупотреблением алкоголем, то заболевание называют неалкогольной жировой болезнью печени (НАЖБП). Чаще всего ей страдают лица с избыточным весом и ожирением, нарушениями в обмене липидов (высоким значением холестерина и/или триглицеридов), сахарным диабетом 2 типа.
К стеатозу печени также приводит систематическое употребление алкоголя в дозах, опасных для здоровья: мужчины — более 30 г алкоголя в день в пересчете на этиловый спирт, женщины — более 20 г алкоголя в день в пересчете на этиловый спирт.
Существуют и более редкие формы стеатоза печени, которые связаны с употреблением некоторых лекарств, генетическими заболеваниями, голоданием с резким похудением, определёнными хирургическими вмешательствами и другими причинами.
Классификация и причины стеатоза печени
Согласно последним исследованиям выделяют следующие основные формы стеатоза печени:
-
в рамках нарушения обмена веществ (метаболической дисфункции), т. е. речь идет о неалкогольной жировой болезни печени, которая может протекать в форме стеатоза;
-
в рамках алкогольной болезни печени;
-
при сочетании двух факторов: отклонений в обмене веществ и употреблении избыточного количества алкоголя;
-
вследствие генетических нарушений (моногенные болезни), например, болезнь Вильсона (нарушение обмена меди);
-
из-за неблагоприятного воздействия на печень некоторых лекарств;
-
причина стеатоза может быть не установлена после тщательного обследования, тогда его называют криптогенным.
Стеатоз печени в рамках неалкогольной жировой болезни печени называют первичным. Наиболее часто НАЖБП сочетается с ожирением, сахарным диабетом 2-го типа, повышенным уровнем холестерина в крови. У таких пациентов стеатоз встречается почти в 95 % случаев. В основе проблемы лежит инсулинорезистентность, т. е. нарушение приема сигналов от гормона инсулина.
Вторичный стеатоз связан с воздействием внешних факторов (например, лекарств, хирургических вмешательств, энергетического дефицита из-за долгого голодания) или генетических заболеваний. Некоторые вирусные инфекции, в частности, хронический гепатит С, тоже сопровождаются стеатозом, который называют вторичным.
При обследовании пациента врач всегда должен исключить все возможные причины стеатоза печени, для этого у него есть диагностические инструменты.
Симптомы стеатоза печени
Проблема в том, что пациенты с НАЖБП на ранних стадиях (стеатоз), как правило, не испытывают никаких ощущений, т. е. заболевание протекает бессимптомно. Если присоединяется воспаление (стеатогепатит), пациент может жаловаться на слабость и повышенную утомляемость, у него могут появиться неприятные ощущения в правом боку. На стадии цирроза печени симптомы отражают его осложнения: асцит (скопление жидкости в животе), отеки, энцефалопатия и другие.
Диагностика стеатоза печени
Обследование пациентов с подозрением на стеатоз печени традиционно начинают с анализов крови:
-
общий клинический анализ крови: как правило, бывает совершенно нормальным;
-
биохимический анализ крови с печёночными пробами может показать небольшое увеличение АЛТ и/или ГГТ (ферментов печени).
Поскольку стеатоз печени очень часто встречается у пациентов с сахарным диабетом 2-го типа и дислипидемией (нарушением обмена жиров), нужно:
-
исследовать уровень глюкозы в крови натощак;
-
при необходимости сделать тест толерантности к глюкозе;
-
изучить гликозилированный гемоглобин, липидограмму с анализом значений «полезного» и «вредного» холестерина.
Поставить окончательный диагноз стеатоза печени помогают:
-
УЗИ органов брюшной полости на основании того, что ткань печени выглядит более «яркой» в сравнении с тканью почки. Также методом УЗИ определяют состояние сосудов и желчных протоков;
-
количественная оценка стеатоза с помощью методики САР, которой оснащен аппарат фиброскан и его аналоги;
-
метод количественной магнитно-резонансной томографии позволяет рассчитать количество жира (FF — fat fraction) в печени наиболее точно. Делают это по значению протонной плотности фракции жира (Proton Density Fat Fraction — PDFF). Это исследование в клинической практике используют редко из-за высокой стоимости и ограниченной доступности;
-
биопсия — самый точный метод исследования печени. Его используют в тех случаях, когда другими способами определить стеатоз не представляется возможным. Помимо стеатоза биопсия дает возможность определить и оценить воспаление и фиброз.
Лечение стеатоза печени
Тактику лечения подбирают в зависимости от причины жирового перерождения печени. Если стеатоз развился из-за злоупотребления алкоголем, его необходимо полностью исключить. Если же заболевание появилось на фоне избыточного веса или ожирения, нужно похудеть и прийти к нормальному индексу массы тела (ИМТ). Доказано, что снижение веса на 10 % от исходного значения помогает существенно уменьшить количество жира в печени и повысить чувствительность к инсулину. Оптимальный ритм похудения — 500 граммов за 10 дней (это приблизительное значение, нужно обязательно высчитывать индивидуально).
Пациентам со стеатозом печени в рамках НАЖБП рекомендуют:
-
умеренные физические нагрузки (прогулки, спортивная ходьба, бег, йога, пилатес);
-
правильное питание (оптимален средиземноморский тип питания; в определённых ситуациях, в частности, при дополнительных отклонениях со стороны желчевыводящей системы, советуют придерживаться диеты №5. Обратите внимание: полностью исключать жиры из питания не нужно, это может навредить здоровью. Оставьте в рационе растительные жиры: они являются источником жирных кислот омега 3;
-
дополнительно к мерам по нормализации образа жизни (физическая активность и правильное питание) назначают гепатотропные препараты, в первую очередь урсодезоксихолевую кислоту (УДХК) — для выведения лишнего жира из клеток печени и уменьшения воспаления, если оно имеет место, улучшения обмена холестерина и свойств желчи. Кроме того, доказано, что УДХК для пациентов с НАЖБП служит профилактикой развития фиброза печени и атеросклероза.
Прогноз и профилактика
Для пациентов со стеатозом печени на ранней стадии прогноз благоприятный при условии устранения причины заболевания (злоупотребления алкоголем, избыточного веса). Предупредить развитие болезни и её осложнений помогают сбалансированное питание, регулярная физическая активность и контроль веса. В отсутствии лечения у больного развивается воспаление — стеатогепатит, что в конечном счёте может привести к необратимым изменениям (цирроз).
Кроме того, при стеатозе печени существенно повышается риск смерти от атеросклеротических заболеваний сердечно-сосудистой системы. По данным исследований, НАЖБП уже на стадии стеатоза служит независимым фактором риска атеросклеротических сердечно-сосудистых заболеваний и их осложнений — инфаркта миокарда и инсульта.
Источники:
-
Подымова С.Д. Жировой гепатоз, неалкогольный стеатогепатит. Клинико-морфологические особенности. Прогноз. Лечение. Приложение РМЖ «Болезни Органов Пищеварения» №2 от 17.02.2005, стр. 61;
-
Rasskazova MA, Vorobyev SV, Butova HN. [Possibilities for the use of ursodeoxycholic acid in the treatment of patients with type 2 diabetes mellitus and non-alcoholic fatty liver disease]. Ter Arkh. 2023 May 31;95(4):316-321. Russian. doi: 10.26442/00403660.2023.04.202125. PMID: 38158979;
-
Ивашкин В.Т., Маевская М.В., Жаркова М.С., Котовская Ю.В., Ткачева О.Н., Трошина Е.А., Шестакова М.В., Маев И.В., Бредер В.В., Гейвандова Н.И., Дощицин В.Л., Дудинская Е.Н., Ершова Е.В., Кодзоева Х.Б., Комшилова К.А., Корочанская Н.В., Майоров А.Ю., Мишина Е.Е., Надинская М.Ю., Никитин И.Г., Погосова Н.В., Тарзиманова А.И., Шамхалова М.Ш. Клинические рекомендации Российского общества по изучению печени, Российской гастроэнтерологической ассоциации, Российской ассоциации эндокринологов, Российской ассоциации геронтологов и гериатров и Национального общества профилактической кардиологии по диагностике и лечению неалкогольной жировой болезни печени. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2022;32(4):104–140. https://doi.org/10.22416/1382-4376-2022-32-4-104-140.











.png)
Авторизуйтесь, чтобы написать комментарий или проголосовать:
Или оставьте его анонимно: